Bí ẩn" về cơ chế của enzyme DICER
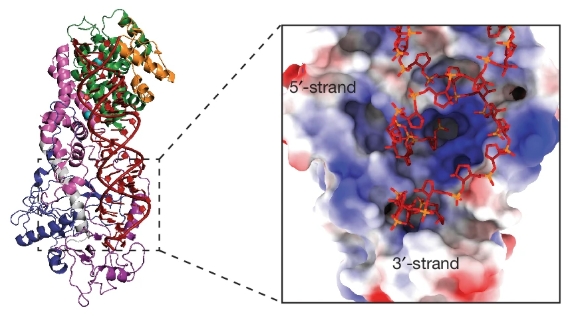
Một nghiên cứu mới đây được công bố trên tạp chí khoa học danh giá Nature đã làm thay đổi những hiểu biết trước đây về cách enzyme DICER xử lý RNA. Bằng việc phát hiện ra một "túi liên kết" thứ hai hoàn toàn mới, các nhà khoa học đã giải mã được cơ chế giúp enzyme này cắt các phân tử RNA với độ chính xác tuyệt đối.
Bối cảnh: "Chiếc kéo" DICER và quy tắc đếm đầu 5'
Cơ chế can thiệp RNA (RNAi) là một quá trình sinh học quan trọng, trong đó cơ thể phụ thuộc vào DICER – một enzyme thiết yếu đóng vai trò như "chiếc kéo" để cắt các tiền chất RNA thành những đoạn RNA điều hòa nhỏ gọn.
Từ trước đến nay, giới khoa học biết rằng DICER thực hiện quá trình cắt dựa trên "quy tắc đếm từ đầu 5'". Cụ thể, enzyme này sẽ đo lường chiều dài của chuỗi RNA bắt đầu từ đầu 5' để xác định chính xác vị trí cần cắt. Tuy nhiên, các nghiên cứu trước đây cho rằng DICER chỉ có duy nhất một túi liên kết ở đầu 5' (túi ưu tiên Uridine - U-favoured) và túi này "kỳ thị" Guanosine (5'-G), từ đó dẫn đến những sai lệch trong quá trình cắt.
Khám phá mới: Phá vỡ quan niệm cũ
Nghiên cứu mới trên Nature đã lật ngược lại quan niệm trên khi chứng minh rằng: 5'-G thực chất lại thúc đẩy quá trình cắt diễn ra vô cùng chính xác đối với rất nhiều cơ chất.
Sử dụng kết hợp các thử nghiệm cắt hàng loạt song song (massively parallel dicing assays) và công nghệ tiên tiến là kính hiển vi điện tử nghiệm lạnh (cryo-EM), nhóm nghiên cứu đã phát hiện ra những điểm mấu chốt sau:
Phát hiện túi liên kết thứ hai: DICER sở hữu một túi liên kết ưu tiên Guanosine (G-favoured) được bảo tồn trong tiến hóa, hoạt động độc lập và hoàn toàn khác biệt so với túi ưu tiên Uridine (U-favoured) đã biết trước đó.
Sự phối hợp hoàn hảo: Sự tồn tại song song của hai túi liên kết này giúp DICER căn chỉnh chính xác vị trí cắt ở các thanh ghi (register) 21-nucleotide và 22-nucleotide, qua đó mở rộng sự hiểu biết về cơ chế sinh tổng hợp RNA nhỏ ở các loài động vật đa bào (metazoan).
Khả năng tự điều chỉnh linh hoạt: Khi xảy ra xung đột giữa việc liên kết đầu 5' và việc nhận diện các dải RNA (RNA-motif), hệ thống sẽ kích hoạt sự thay đổi hình thái của RNA để bảo toàn việc lựa chọn đúng vị trí cắt.
Chuyển động của các miền cấu trúc: Các miền liên kết RNA chuỗi kép (dsRBD) và miền PAZ của enzyme cũng tự điều chỉnh cấu trúc để giúp cơ chất khớp hoàn hảo với trung tâm xúc tác, đảm bảo việc cắt chuỗi kép diễn ra chính xác nhất.
Ý nghĩa của nghiên cứu
Nghiên cứu này là một bước tiến lớn trong sinh học phân tử. Nó khẳng định rằng cơ chế cắt của DICER là một hệ thống phức tạp và tinh vi, tích hợp giữa túi liên kết kép ở đầu 5', sự chi phối của các dải RNA, và chuyển động linh hoạt của các miền cấu trúc.
Kết quả này không chỉ giải quyết được những mâu thuẫn trong các tài liệu sinh học trước đây mà còn mở ra nền tảng vững chắc để hiểu sâu hơn về quá trình sinh tổng hợp microRNA – một yếu tố then chốt trong việc điều hòa gen và có liên quan mật thiết đến nhiều căn bệnh ở người, bao gồm cả ung thư.
Link chi tiết: https://www.nature.com/articles/s41586-026-10211-5
Bối cảnh: "Chiếc kéo" DICER và quy tắc đếm đầu 5'
Cơ chế can thiệp RNA (RNAi) là một quá trình sinh học quan trọng, trong đó cơ thể phụ thuộc vào DICER – một enzyme thiết yếu đóng vai trò như "chiếc kéo" để cắt các tiền chất RNA thành những đoạn RNA điều hòa nhỏ gọn.
Từ trước đến nay, giới khoa học biết rằng DICER thực hiện quá trình cắt dựa trên "quy tắc đếm từ đầu 5'". Cụ thể, enzyme này sẽ đo lường chiều dài của chuỗi RNA bắt đầu từ đầu 5' để xác định chính xác vị trí cần cắt. Tuy nhiên, các nghiên cứu trước đây cho rằng DICER chỉ có duy nhất một túi liên kết ở đầu 5' (túi ưu tiên Uridine - U-favoured) và túi này "kỳ thị" Guanosine (5'-G), từ đó dẫn đến những sai lệch trong quá trình cắt.
Khám phá mới: Phá vỡ quan niệm cũ
Nghiên cứu mới trên Nature đã lật ngược lại quan niệm trên khi chứng minh rằng: 5'-G thực chất lại thúc đẩy quá trình cắt diễn ra vô cùng chính xác đối với rất nhiều cơ chất.
Sử dụng kết hợp các thử nghiệm cắt hàng loạt song song (massively parallel dicing assays) và công nghệ tiên tiến là kính hiển vi điện tử nghiệm lạnh (cryo-EM), nhóm nghiên cứu đã phát hiện ra những điểm mấu chốt sau:
Phát hiện túi liên kết thứ hai: DICER sở hữu một túi liên kết ưu tiên Guanosine (G-favoured) được bảo tồn trong tiến hóa, hoạt động độc lập và hoàn toàn khác biệt so với túi ưu tiên Uridine (U-favoured) đã biết trước đó.
Sự phối hợp hoàn hảo: Sự tồn tại song song của hai túi liên kết này giúp DICER căn chỉnh chính xác vị trí cắt ở các thanh ghi (register) 21-nucleotide và 22-nucleotide, qua đó mở rộng sự hiểu biết về cơ chế sinh tổng hợp RNA nhỏ ở các loài động vật đa bào (metazoan).
Khả năng tự điều chỉnh linh hoạt: Khi xảy ra xung đột giữa việc liên kết đầu 5' và việc nhận diện các dải RNA (RNA-motif), hệ thống sẽ kích hoạt sự thay đổi hình thái của RNA để bảo toàn việc lựa chọn đúng vị trí cắt.
Chuyển động của các miền cấu trúc: Các miền liên kết RNA chuỗi kép (dsRBD) và miền PAZ của enzyme cũng tự điều chỉnh cấu trúc để giúp cơ chất khớp hoàn hảo với trung tâm xúc tác, đảm bảo việc cắt chuỗi kép diễn ra chính xác nhất.
Ý nghĩa của nghiên cứu
Nghiên cứu này là một bước tiến lớn trong sinh học phân tử. Nó khẳng định rằng cơ chế cắt của DICER là một hệ thống phức tạp và tinh vi, tích hợp giữa túi liên kết kép ở đầu 5', sự chi phối của các dải RNA, và chuyển động linh hoạt của các miền cấu trúc.
Kết quả này không chỉ giải quyết được những mâu thuẫn trong các tài liệu sinh học trước đây mà còn mở ra nền tảng vững chắc để hiểu sâu hơn về quá trình sinh tổng hợp microRNA – một yếu tố then chốt trong việc điều hòa gen và có liên quan mật thiết đến nhiều căn bệnh ở người, bao gồm cả ung thư.
Link chi tiết: https://www.nature.com/articles/s41586-026-10211-5
